General Tools LTM2X Laser-Maßband, 2-in-1, 1,8 m Laser-Maßband und 4,8 m Maßband mit großem, leicht ablesbarem digitalem Display, blau (LTM2X-BL-Q) : Amazon.de: DIY & Tools

Laser-entfernungsmesser Elektronisches Roulette Laser Digitales Maßband Entfernungsmesser Trena Subway Laser-entfernungsmesser Metrisches/imperiales Maßband | Kaufen Sie Die Neuesten Trends | Temu Germany

larissastoffe Maßband Profi Maßband, Schneidermaßband, Bandmaß, 150 cm 10 mm, 150 cm x 1,0 cm, Made in Germany

SNDWAY laser-entfernungsmesser 40M 60M digitale maßband digitale maßband laser werkzeug SW-TM40 - AliExpress

BMI Taschenbandmaß - meter, 3m, rot mm/mm mit Stopper und Clip - SB-verpackt 429341021 4007368104964 ToolTeam T-44737

Laser Messgerät Massband, Digitales Laserdistanzmessgerät mit LCD -Display, Lasermessung 196 ft, Maßband 16 ft : Amazon.de: Baumarkt

SNDWAY laser-entfernungsmesser 40M 60M digitale maßband digitale maßband laser werkzeug SW-TM40 - AliExpress

GTA 40m Laser Maßband 3 in 1 Ranger Digital Finder 5m Maßband Multifunktions-Lasermaß Datenspeicher, Blau

Maßband 2 In 1 Digitales Massband Laser Entfernungsmesser Laser-bandmaß Laser Messung 131ft/40m, Maßband 16ft/5m Mit LCD Hintergrundbeleuchtung Wiederaufladbares Laser-distanzmessgerät : Amazon.de: Baumarkt

Kreuzlinienlaser Universal Level, Massband Laser Entfernungsmesser 2 in 1, 550cm Maßband, Dicker Glatter Aluminiumboden : Amazon.de: Baumarkt

Gear X 5m Maßband mit 30m Laser (schwarz, ABS, Edelstahl, 193g) als Werbegeschenke Auf GIFFITS.de | Art.Nr. 464338

Massband Laser Entfernungsmesser, 3 in 1 Digitales Laser-bandmaß Laser Messung 40m, Maßband 5m mit LCD Hintergrundbeleuchtung Laser Distanzmessgerät für Flächen/Volumen : Amazon.de: Baumarkt

Massband Laser Entfernungsmesser, 2 in 1 digitales Laser-bandmaß Laser messung 131ft/40m, maßband 16ft/5m mit LCD Hintergrundbeleuchtung wiederaufladbares Laser-Distanzmessgerät für Flächen/Volumen : Amazon.de: Baumarkt

30 mt Laser-entfernungsmesser Digitale Maßband Abstand Meter 5 mt Tragbare Einziehbare Klebeband Lineal IP54 Infrarot Bau Werkzeuge - AliExpress

Gear X 5m Maßband mit 30m Laser (schwarz, ABS, Edelstahl, 193g) als Werbegeschenke Auf GIFFITS.de | Art.Nr. 464338

40M Laser Maßband Abstand Meter Edelstahl Digitale Versenkbare Rolle Schnur Entfernungsmesser Holzbearbeitung Laser-Mess Werkzeug

Gear X 5m Maßband mit 30m Laser (schwarz, ABS, Edelstahl, 193g) als Werbegeschenke Auf GIFFITS.de | Art.Nr. 464338
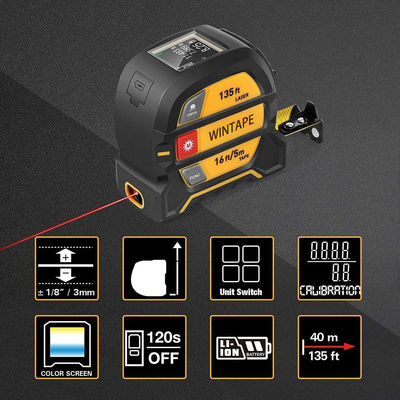
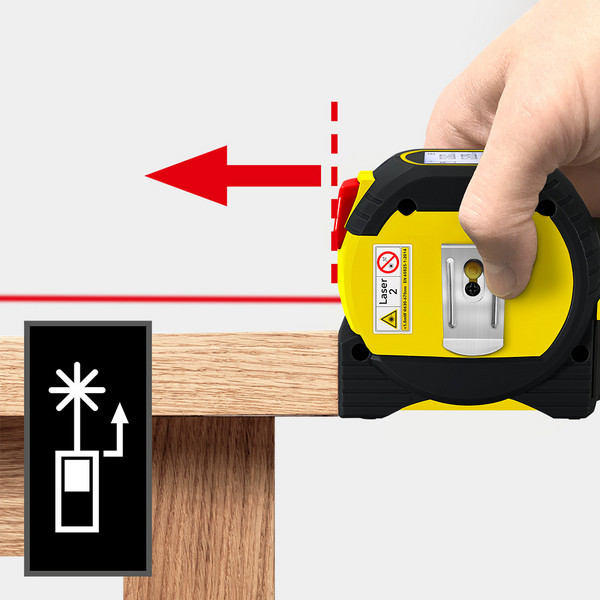
WINTAPE 131 Fuß digitales Laser-Maßband Home Depot Digitales Maßband mit seitlichem Laser-Autolock. Normales Maßband

1 Stk. Laser-bandmaß 3 In 1 Digitales Bandmaß Hochpräzisions-laser-entfernungsmesser Stahlbandmaß - Werkzeuge & Heimwerkerbedarf - Temu Germany

Semlos Laser Wasserwaage kreuzlinienlaser Bandmaß 250cm Stahlmaßstab Wasserwaage (Nicht Geeignet für den Einsatz bei Starker Sonneneinstrahlung) : Amazon.de: Baumarkt

HOTO Laser Maßband, Smart Laser-entfernungsmesser, Intelligente, 30M, OLED Display, laser Abstand Meter, Verbinden Zu APP

Laser-entfernungsmesser Elektronisches Roulette Laser Digitales Maßband Entfernungsmesser Trena Subway Laser-entfernungsmesser Metrisches/imperiales Maßband | Kaufen Sie Die Neuesten Trends | Temu Germany

Handlaser-Maßband, Laser-Maßband, Korrosionsbeständig, Digital für den Bau (60m) : Amazon.de: Baumarkt

1 Stk. Laser-bandmaß 3 In 1 Digitales Bandmaß Hochpräzisions-laser-entfernungsmesser Stahlbandmaß - Werkzeuge & Heimwerkerbedarf - Temu Germany

WINTAPE 131 Fuß digitales Laser-Maßband Home Depot Digitales Maßband mit seitlichem Laser-Autolock. Normales Maßband

3 in 1 Laser Abstand Meter Mess Laser Maßband Digitale Laser-entfernungsmesser Digitale Elektronische Roulette Edelstahl 5m Band - AliExpress

Gear X 5m Maßband mit 30m Laser (schwarz, ABS, Edelstahl, 193g) als Werbegeschenke Auf GIFFITS.de | Art.Nr. 464338